江蘇單抗藥物用宿主細胞蛋白(HCP)殘留檢測橋接驗證
來源:
發(fā)布時間:2025-12-05
中國倉鼠卵巢細胞(Chinese Hamster Ovary,CHO)是生物制品生產(chǎn)中常用的動物細胞表達系統(tǒng),廣泛應(yīng)用于抗體、重組蛋白、疫苗等產(chǎn)品的制備。采用 CHO 細胞作為宿主進行生產(chǎn)時,難免會引入宿主細胞蛋白(HCP)雜質(zhì);即便 HCP 殘留量較低,仍可能存在免疫原性,還會帶來降低產(chǎn)品蛋白穩(wěn)定性等風(fēng)險。因此,需對生物制品中的 HCP 殘留進行定量分析,從而保障純化工藝的一致性與終產(chǎn)品的安全性。SHENTEK®CHO 宿主細胞蛋白(HCP )殘留檢測試劑盒實現(xiàn)了關(guān)鍵試劑的全國產(chǎn)化,其通過 CHO 細胞(K1&S)補料分批培養(yǎng)工藝制備 HCPs,再以此免疫綿羊獲取抗體,適用于檢測 CHO 細胞系表達的生物制品(如單抗、重組蛋白、疫苗等)中的 HCP 殘留。該試劑盒具有操作步驟少、檢測速度快、專一性強、性能穩(wěn)定可靠的特點。
相關(guān)數(shù)據(jù)顯示,定制化 HCP 檢測試劑盒檢測值高于商業(yè)化產(chǎn)品,更契合產(chǎn)品質(zhì)量控制需求。江蘇單抗藥物用宿主細胞蛋白(HCP)殘留檢測橋接驗證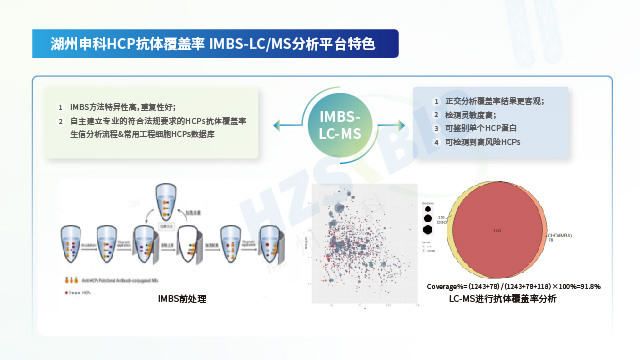
宿主細胞蛋白(HCP)多與細胞關(guān)鍵功能相關(guān),例如細胞增殖、基因轉(zhuǎn)錄、蛋白合成修飾、細胞存活及凋亡等,在生產(chǎn)工藝中會因細胞分泌、死亡或裂解而釋放。生產(chǎn)過程里,有三大因素主要影響 HCP 的組成與豐度:①宿主細胞基因組調(diào)控及培養(yǎng)工藝:特定工藝下,潛在 HCP 數(shù)量可能極多,且并非所有基因都會表達,部分基因的表達具有時間和條件特異性;像大腸桿菌約含 4300 個基因,不同工藝產(chǎn)物會經(jīng)歷獨特的翻譯后修飾,這增加了 HCP 的總數(shù)與生化復(fù)雜性。研究顯示,大腸桿菌表達的蛋白間存在數(shù)量差異,這種差異可能是對環(huán)境條件的適應(yīng)性反應(yīng),但 85-90% 具有潛在免疫原性的 HCP 在不同發(fā)酵過程中均會出現(xiàn)。②產(chǎn)物表達方式:宿主細胞與外源基因、載體及輔助成分構(gòu)成的體系,可實現(xiàn)穩(wěn)定、瞬時及誘導(dǎo)表達;以大腸桿菌為例,常見表達形式包括胞內(nèi)表達、分泌表達、可溶性表達、不溶性包涵體形式,還有融合與非融合表達。③純化步驟及產(chǎn)品自身特性的影響:純化過程中能去除 99% 以上的 HCP,但仍有少量殘留 HCP 留在產(chǎn)品中,這些殘留 HCP 可能與產(chǎn)品結(jié)合,隨產(chǎn)品一同被純化。
成都單抗藥物用宿主細胞蛋白(HCP)殘留檢測不同技術(shù)平臺獲得的抗體覆蓋率水平不一樣,一般覆蓋率水平從高到低依次IMBS-MS>IMBS-2D>2D-Western Blot。
憑借高分辨質(zhì)譜技術(shù),湖州申科生物推出宿主細胞蛋白定制化檢測服務(wù)組合,可滿足生物制品殘留蛋白的分析需求。該平臺服務(wù)內(nèi)容包括:1、HCP蛋白檢測定制化服務(wù):借助ELISA、雙向電泳(2D)與LC-MS/MS技術(shù),為常規(guī)生物制品檢測、高危及工藝相關(guān)蛋白數(shù)據(jù)庫搭建、特殊生物制品分析提供支持;2、抗體覆蓋率服務(wù):運用自主研發(fā)的IMBS技術(shù)結(jié)合質(zhì)譜,準確評估ELISA試劑盒對工程細胞HCP的捕獲能力,同時完成校準品表征;3、靶向HCP檢測:專注于高風(fēng)險殘留蛋白的檢測方法開發(fā);4、蛋白種屬鑒定服務(wù):利用LC-MS技術(shù)追溯樣品中的物種特異性肽段。該服務(wù)體系以多技術(shù)聯(lián)用和深度定制化策略為支撐,可滿足從基礎(chǔ)篩查到工藝關(guān)鍵雜質(zhì)監(jiān)控的全維度需求。
宿主細胞殘留蛋白(HCP)檢測是生物制品質(zhì)量控制的關(guān)鍵環(huán)節(jié),當(dāng)前主流技術(shù)為基于抗體的免疫學(xué)方法(如 ELISA)。但實際檢測中,不同試劑盒的結(jié)果常存在明顯偏差,關(guān)鍵問題源于其兩大關(guān)鍵組分 ——HCP 校準品與檢測抗體 —— 在制備及表征上的高度可變性。作為定量基準的校準品,自身復(fù)雜性極高。不同供應(yīng)商制備時,所用細胞來源、培養(yǎng)及表達條件存在明顯差異,且宿主蛋白的提取純化工藝(如目標產(chǎn)物去除策略)也各不相同,這些差異直接導(dǎo)致校準品的組成、對實際樣品的代表性及儲存穩(wěn)定性千差萬別。檢測抗體(尤其是多克隆抗體)需通過免疫動物獲得,其特異性與 HCP 覆蓋度受多重因素影響:免疫原的選擇、動物個體免疫應(yīng)答差異、免疫方案設(shè)計,以及后續(xù)抗體篩選與純化流程,都會讓不同批次或來源的抗體,在對不同 HCP 的親和力、對低豐度蛋白的檢測靈敏度等識別譜特性上,形成本質(zhì)區(qū)別。
湖州申科開發(fā)多種宿主 HCP 檢測試劑盒,提供抗體覆蓋率驗證服務(wù)。
為何定制化試劑盒是宿主細胞蛋白(HCP)殘留檢測的優(yōu)先選擇?特定工藝來源的抗原與校準品更具代表性,是重要原因之一。不同生物制品的上游生產(chǎn)工藝存在差異,比如培養(yǎng)基、培養(yǎng)條件、收獲時機等不同,都會使產(chǎn)生的 HCP 在蛋白種類、豐度及翻譯修飾上出現(xiàn)區(qū)別,進而導(dǎo)致進入下游純化工藝的 HCP 類型相應(yīng)改變 —— 尤其是與藥物主成分共同純化的 HCP,會以優(yōu)勢蛋白的形式存在于藥物原液或制劑中。HCP 定制化 ELISA 檢測試劑盒通常選用實際生產(chǎn)工藝中上游發(fā)酵后的樣品制備抗原與校準品,這樣制得的校準品能較充分地體現(xiàn)實際工藝中的 HCP,有效降低因抗原或校準品種類不足引發(fā)的漏檢風(fēng)險,同時減少定量不準確的問題。
憑借凍干保存技術(shù),湖州申科 HCP 試劑盒校準品穩(wěn)定性超 10 年,筑牢長期供應(yīng)基礎(chǔ)。HEK293宿主細胞蛋白(HCP)殘留檢測方法開發(fā)不同培養(yǎng)工藝和產(chǎn)物表達影響 HCP 的數(shù)量和生化復(fù)雜性。江蘇單抗藥物用宿主細胞蛋白(HCP)殘留檢測橋接驗證
HCP 是宿主細胞(多為哺乳動物細胞或微生物)所產(chǎn)生的蛋白質(zhì),這類蛋白質(zhì)存在潛在風(fēng)險,可能對藥物的安全性與有效性產(chǎn)生影響。因此,宿主細胞蛋白(HCP )殘留量成為生物藥物的關(guān)鍵質(zhì)量屬性,需在藥物開發(fā)與生產(chǎn)階段,對 HCP 的存在進行嚴格監(jiān)控、管理并做好記錄。隨著生產(chǎn)流程推進,生物制品純度逐步提升,但 HCP 的總量與種類也在不斷減少,這無疑增加了 HCP 分析與監(jiān)測工作的難度。在此背景下,開發(fā)高效的 HCP 富集材料及技術(shù)便顯得尤為重要。低豐度宿主殘留蛋白富集試劑盒,專為富集生物制品(如單抗、融合蛋白等)中的 HCP 并去除高豐度蛋白而設(shè)計,其通過磁珠法構(gòu)建多樣化且復(fù)雜的親和配體庫,以實現(xiàn)對目標蛋白的高效識別與結(jié)合。該試劑盒的設(shè)計不僅覆蓋傳統(tǒng)單一蛋白,還可適配融合蛋白、單克隆抗體等多種生物樣本類型,體現(xiàn)出較強的適用性與靈活性。江蘇單抗藥物用宿主細胞蛋白(HCP)殘留檢測橋接驗證
上一篇
山西合規(guī)性熱原檢測
相關(guān)新聞
- 四川疫苗產(chǎn)品支原體檢測技術(shù)服務(wù) 2025-12-05
- 江蘇CHO宿主細胞蛋白(HCP)殘留檢測試劑盒 2025-12-05
- 浙江疫苗產(chǎn)品支原體檢測指示細胞培養(yǎng)法 2025-12-05
- 廣東免疫細胞產(chǎn)品支原體檢測可比性驗證 2025-12-05
- 重慶重組藥物支原體檢測NAT法 2025-12-05
- 廣東免疫細胞產(chǎn)品支原體檢測國產(chǎn)替代 2025-12-05
- 浙江CHO宿主細胞蛋白(HCP)殘留檢測 2025-12-05
- 河北復(fù)雜基質(zhì)支原體檢測方法學(xué)驗證 2025-12-05
- 江西干細胞產(chǎn)品支原體檢測技術(shù)服務(wù) 2025-12-05
- 上海細胞療法產(chǎn)品支原體檢測技術(shù)服務(wù) 2025-12-05
推薦新聞
- 鼓樓區(qū)健康管理咨詢大概多少錢 2025-12-06
- 福建單人民用氧艙廠家電話 2025-12-06
- 拱墅區(qū)比較好的顯微鏡 2025-12-06
- 廣東細胞保存液值得推薦 2025-12-06
- 睪酮 ELISA 試劑盒 2025-12-06
- 湖北滅菌咽拭子生產(chǎn)廠家 2025-12-06
- 安徽實驗分析儀器歡迎選購 2025-12-06
- 青海哪里有包埋 2025-12-06
- 云貴川腎結(jié)石體外震波碎石機招標 2025-12-06
- 青海cas號33135-50-1PLLA左旋聚乳酸醫(yī)院采購 2025-12-06