天津疫苗產品支原體檢測培養法
來源:
發布時間:2025-12-04
為解決支原體檢測的污染難題,湖州申科推出AdvSHENTEK® 外源因子全自動核酸檢測分析系統 + 一體化支原體檢測卡盒的組合方案,以全封閉設計從根源規避污染。該方案只需一步開蓋加樣,后續流程完全封閉運行,物理隔絕核酸氣溶膠污染,搭配 UNG 酶系統可進一步防止環境交叉污染,能節省 100% 污染排查時間。一體化檢測卡盒相當于單獨的迷你 qPCR 實驗室,集成試劑準備、樣品制備、擴增、分析全流程,無需復雜分區。同時,方案降低了對實驗環境和人員的要求,普通實驗室即可開展檢測,人員經簡單培訓就能操作,徹底擺脫了傳統 NAT 法對高技能人員和場地的依賴,大幅提升檢測結果的穩定性。
湖州申科支原體驗證菌株溯源至 ATCC/CVCC,標定 10CFU/100CFU,滿足驗證需求。天津疫苗產品支原體檢測培養法
湖州申科圍繞 USP 支原體培養法,提供技術服務,滿足生物制劑企業的合規需求。服務內容包括兩項:一是支原體培養法樣品檢測服務,嚴格遵循 USP 63 標準流程執行,確保檢測結果合規有效;二是支原體培養法樣品適用性驗證服務,針對供試品特性開展定制化驗證,保障檢測方法與樣品的適配性。所有檢測與驗證完成后,公司將出具標準化報告,報告可直接用于項目申報、審批、工藝優化等場景,為企業產品質量控制提供依據。通過專業的技術服務,幫助企業規避合規風險,確保生物制劑生產全流程的質量與安全性,助力企業高效推進產品研發與上市進程。
江蘇疫苗產品支原體檢測核酸擴增法全血基質中100 CFU/mL支原體,湖州申科支原體檢測試劑盒通過優化提取流程實現穩定擴增與檢出。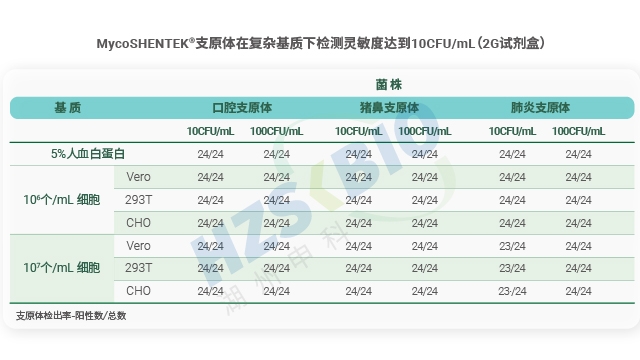
陰性翹尾是支原體 NAT 檢測中常見的異常現象,表現為 NCS 或 NTC 出現擴增信號,Ct 值多在 35~40 之間,需科學評估并處理。首先考慮污染因素,可能是陰性對照被陽性樣本、試劑或環境氣溶膠污染,建議立即復測,復測時使用帶濾芯低吸附 TIP 頭,嚴格執行陰陽性分區操作,注重細節防控。其次需排除背景信號等非典型性擴增的干擾,避免誤判為污染。若前期驗證中頻繁出現 NTC 或 NCS 擴增,且已徹底排除污染可能性,可結合已有實驗數據重新設置 Cut off 值,確保閾值線能有效區分真實陽性與背景信號,滿足實驗室檢測需求。
全球主流藥典均認可 NAT 法作為支原體檢測的替代方法,但明確要求需經過充分驗證并證明與傳統方法的可比性。歐洲藥典(EP)2.6.7 規定 NAT 法可作為替代方法,需開展供試品抑制性驗證;美國藥典(USP)63&77 要求替代方法需與培養法、指示細胞培養法均具備可比性,且 USP<77> 專門針對支原體 NAT 法的驗證與檢測制定了規范;日本藥典(JP)G3-14-170 允許經適當驗證后的 NAT 法替代傳統方法;中國藥典 3301 及相關指導原則明確,CAR-T、干細胞等新型產品可采用 NAT 法,但需充分驗證其最低檢出限不低于藥典方法,早期需與藥典方法并行使用。此外,各國法規均強調,NAT 法的選擇、開發與應用需基于科學依據,充分考慮培養基、生產工藝、潛在污染菌株等因素。
支原體檢測試劑盒批間穩定性至關重要,需通過多批次驗證確保質量均一。
選擇合適的商業化支原體試劑盒需綜合五大主要維度,確保檢測合規、穩定與高效。一是監管認可度,需關注試劑盒驗證的全面性與室間驗證情況,菌株選擇是否合規,以及廠家是否有豐富的客戶申報案例;二是廠家資質,確認廠家是否接受供應商審計,能否提供 “產品 + 服務” 的全流程解決方案;三是產品設計,重點考察試劑盒方法學驗證的嚴謹性、對復雜樣品基質的耐用性與抗干擾能力,以及是否具備避免假陰 / 假陽性的質控設計,是否符合藥典要求;四是技術支持,評估廠家的技術響應速度、問題解決能力,能否提供專業的驗證指導;五是質量保障,關注試劑盒供應的穩定性與質量均一性,避免因產品批次差異影響檢測結果,確保長期質控需求的穩定滿足。
細胞庫(MCB/WCB)需每 2-4 周監測支原體,保障生產起始環節安全。重組藥物支原體檢測NAT法細胞療法產品時效短,需用 核酸擴增NAT 法快速檢測支原體,滿足放行時效。天津疫苗產品支原體檢測培養法
此前,支原體檢測依賴培養法和指示細胞培養法,這兩種傳統方法均被各國藥典列為基礎檢測手段,但存在明顯短板。培養法作為 “金標準”,需陽性活菌參照,每批次培養基需做靈敏度測試,完整合規檢測周期長達 21-35 天;指示細胞培養法同樣耗時 14-28 天,難以滿足新型生物制品快速上市、短貨架期的放行需求。更棘手的是,面對高蛋白等復雜樣品基質,傳統方法易受干擾或抑制,需額外增加傳代培養步驟,導致檢測時間再延長 2-3 周,嚴重影響生產效率,也難以適配新型生物制品的檢測場景。
天津疫苗產品支原體檢測培養法
上一篇
血液制品內毒素檢測抗干擾方案
下一篇:
上海復雜基質支原體檢測NAT法
相關新聞
- 四川疫苗產品支原體檢測技術服務 2025-12-05
- 江蘇CHO宿主細胞蛋白(HCP)殘留檢測試劑盒 2025-12-05
- 浙江疫苗產品支原體檢測指示細胞培養法 2025-12-05
- 廣東免疫細胞產品支原體檢測可比性驗證 2025-12-05
- 重慶重組藥物支原體檢測NAT法 2025-12-05
- 廣東免疫細胞產品支原體檢測國產替代 2025-12-05
- 浙江CHO宿主細胞蛋白(HCP)殘留檢測 2025-12-05
- 河北復雜基質支原體檢測方法學驗證 2025-12-05
- 江西干細胞產品支原體檢測技術服務 2025-12-05
- 上海細胞療法產品支原體檢測技術服務 2025-12-05
推薦新聞
- 工業園區標準聚醚醚酮 2025-12-06
- 安徽國產助腿器服務熱線 2025-12-06
- 燕麥纖維中恩特膳 2025-12-06
- 東莞古法今制養生茶加盟連鎖店 2025-12-06
- 海南是什么助膝器旅游 2025-12-06
- 高新區提供一次性注射器銷售電話 2025-12-06
- 江西國內助踝器加盟連鎖店 2025-12-06
- 西湖區生物檢測試劑盒 2025-12-06
- 安徽包含什么手術無影燈生產企業 2025-12-06
- 河北是什么安思爾成交價 2025-12-06