E.coli表達菌宿主細胞蛋白(HCP)殘留檢測試劑盒
來源:
發(fā)布時間:2025-11-27
湖州申科生物依托先進的整合技術(shù)平臺,在 HCP 檢測領(lǐng)域構(gòu)筑優(yōu)勢。公司自主研發(fā)出突破性技術(shù),包括基于 IMBS 的抗體覆蓋率檢測方法與基于核酸文庫的低豐度 HCP 富集技術(shù),有效提升 HCP 檢測靈敏度與抗體覆蓋能力,相關(guān)成果已在《中國新藥雜志》《藥物分析雜志》等期刊發(fā)表,且被納入國家科技重大專項。同時,借助前沿的精密分析平臺,湖州申科打造了覆蓋完整 HCP 分析鏈條的 LC-MS 解決方案,涵蓋抗原一致性評價、IMBS 前處理、低豐度蛋白富集、生信分析及專屬數(shù)據(jù)庫構(gòu)建等關(guān)鍵環(huán)節(jié),構(gòu)建起從樣品管理到風(fēng)險分析的閉環(huán)體系。該平臺嚴(yán)格遵循法規(guī)要求,所有檢測技術(shù)均通過符合 ICH 及藥典標(biāo)準(zhǔn)的方法學(xué)驗證,確保檢測數(shù)據(jù)可靠,且滿足生物制品申報(如 IND/BLA)的法規(guī)要求。憑借這一技術(shù)整合能力,公司已為國內(nèi)外上百家生物醫(yī)藥企業(yè)提供從工藝開發(fā)到質(zhì)控放行的一站式 HCP 檢測服務(wù),助力單抗、疫苗等產(chǎn)品提升安全性與合規(guī)性。
HCP具有異質(zhì)性,體現(xiàn)在分子本身的多樣性以及和工藝相關(guān)的變異性。E.coli表達菌宿主細胞蛋白(HCP)殘留檢測試劑盒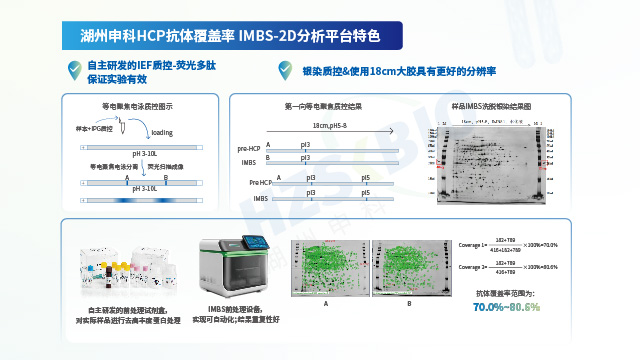
宿主細胞蛋白(HCP)是生物制品中源自細胞基質(zhì)的殘留雜質(zhì),異質(zhì)性特征明顯。其復(fù)雜性主要體現(xiàn)在三方面:①理化特性差異:包含胞內(nèi)與分泌蛋白(涉及關(guān)鍵生理功能),等電點(pI 3-11)、分子量(5-250kDa)及疏水性的區(qū)間跨度大;②上游工藝影響:不同發(fā)酵工藝(如細胞株選擇、培養(yǎng)條件控制)會誘導(dǎo)獨特的翻譯后修飾(PTM),進而增加 HCP 的總量與生化復(fù)雜性;③下游工藝與產(chǎn)物特性干擾:抗體、細胞因子等重組蛋白或病毒類藥物的純化工藝,會選擇性殘留特定 HCP;同時,產(chǎn)物形式(如大腸桿菌的包涵體 / 可溶性表達)也會直接影響 HCP 的殘留譜。針對特定生產(chǎn)工藝開發(fā)定制化檢測方案,是準(zhǔn)確監(jiān)控 HCP 殘留的關(guān)鍵所在。
畢赤酵母宿主細胞蛋白(HCP)殘留檢測方法學(xué)驗證湖州申科全自動 HCP ELISA 系統(tǒng)實現(xiàn)從加樣到檢測自動化,提升效率。
宿主細胞蛋白(HCP)殘留監(jiān)測是生物藥物生產(chǎn)中的關(guān)鍵質(zhì)量屬性(Critical Quality Attribute, CQA),需在藥物開發(fā)與生產(chǎn)階段對 HCP 的存在實施嚴(yán)格監(jiān)控、管理及記錄。隨著生產(chǎn)流程推進,生物制品目標(biāo)蛋白純度逐步提升,HCP 含量則相應(yīng)持續(xù)下降,這導(dǎo)致對單抗、融合蛋白等富含目標(biāo)蛋白的下游工藝樣品進行 HCP 分析監(jiān)測時,難度明顯增加。在此背景下,高效的 HCP 富集材料與技術(shù)顯得尤為重要。SHENTEK®AbunProteoX 是基于磁珠構(gòu)建的親和配體,能高效識別并結(jié)合目標(biāo)蛋白;借助磁性納米顆粒的獨特特性,它可快速高效捕獲 HCP,大幅提升檢測靈敏度。此外,該親和配體的普遍適用性,讓 AbunProteoX 處理多種生物樣本時表現(xiàn)優(yōu)異,可確保樣品中存在高濃度目標(biāo)蛋白時,對低濃度 HCP 的質(zhì)譜、電泳等檢測分析具備準(zhǔn)確性與可靠性。
湖州申科生物憑借自主可控的供應(yīng)鏈與經(jīng)嚴(yán)格驗證的技術(shù)性能,確保 HCP 檢測試劑盒的長期穩(wěn)定供應(yīng)及出色分析能力。一方面,公司實現(xiàn)關(guān)鍵物料自研自產(chǎn):校準(zhǔn)品通過凍干工藝大規(guī)模生產(chǎn),能穩(wěn)定儲存 10 年以上;抗體經(jīng)大動物免疫制備,產(chǎn)量可支撐≥10,000 盒試劑盒生產(chǎn),確保同批次抗體連續(xù)供應(yīng)超 10 年;試劑盒經(jīng)多批次驗證,批內(nèi)與批間一致性表現(xiàn)良好。另一方面,所有產(chǎn)品均參照 ICH Q2(R2)及 ICH M10 法規(guī)要求完成驗證:以大腸桿菌(E.coli)HCP 產(chǎn)品為例,其線性范圍(1-243 ng/mL)的 R2>0.999,各濃度點回收率偏差≤5%;準(zhǔn)確度處于 81.2%-111.6% 區(qū)間,中間精密度 CV 值為 5.7%-12.4%;定量限(LLOQ)低至 1.5 ng/mL,且對 CHO、HEK293 等多種宿主細胞的交叉反應(yīng)均低于檢測限。同時,借助二維電泳(檢出 826 個蛋白點)與質(zhì)譜法(鑒定 2204 個蛋白點)對校準(zhǔn)品進行雙重表征,并運用 IMBS-2D(覆蓋率 > 70%)與 IMBS-MS(覆蓋率 84.7%)正交技術(shù)驗證抗體覆蓋率,從源頭保障檢測結(jié)果的全面性與可靠性。
樣品與抗體的匹配程度對宿主細胞蛋白殘留檢測的結(jié)果影響很大。
LC-MS/MS 作為成熟穩(wěn)定的蛋白質(zhì)組學(xué)分析技術(shù),依托超高分辨率與準(zhǔn)確度,在生物分析領(lǐng)域中占據(jù)關(guān)鍵地位。該技術(shù)不僅可對低含量宿主細胞殘留蛋白(HCP)開展定性檢測,還能通過構(gòu)建專屬蛋白質(zhì)譜庫準(zhǔn)確鑒定 HCP 的具體種類,為深度解析殘留蛋白組成提供重要支撐。不過該技術(shù)應(yīng)用中面臨的主要挑戰(zhàn),是如何優(yōu)化 LC-MS 方法以契合 GMP 規(guī)范對產(chǎn)品放行檢測的嚴(yán)苛要求。在質(zhì)譜檢測環(huán)節(jié),引入表征明確的內(nèi)標(biāo)與外標(biāo)蛋白,可準(zhǔn)確分析 HCPs 的整體組成,并有效識別其中具有潛在風(fēng)險的高風(fēng)險蛋白。這一技術(shù)手段不僅為開發(fā)產(chǎn)品專屬 HCP ELISA 檢測方法提供有力數(shù)據(jù)支撐,還可助力工藝優(yōu)化升級,加快推進生物制品從研發(fā)到獲批上市的全流程進度。
宿主細胞蛋白殘留檢測試劑盒的開發(fā)不是一個簡單的過程,是一個對平臺、技術(shù)均有很高要求的整體流程。E.coli表達菌宿主細胞蛋白(HCP)殘留檢測試劑盒不同技術(shù)平臺獲得的抗體覆蓋率水平不一樣,一般覆蓋率水平從高到低依次IMBS-MS>IMBS-2D>2D-Western Blot。E.coli表達菌宿主細胞蛋白(HCP)殘留檢測試劑盒
宿主細胞殘留蛋白(HCP)檢測是生物制品質(zhì)量控制的關(guān)鍵環(huán)節(jié),當(dāng)前主流技術(shù)為基于抗體的免疫學(xué)方法(如 ELISA)。但實際檢測中,不同試劑盒的結(jié)果常存在明顯偏差,關(guān)鍵問題源于其兩大關(guān)鍵組分 ——HCP 校準(zhǔn)品與檢測抗體 —— 在制備及表征上的高度可變性。作為定量基準(zhǔn)的校準(zhǔn)品,自身復(fù)雜性極高。不同供應(yīng)商制備時,所用細胞來源、培養(yǎng)及表達條件存在明顯差異,且宿主蛋白的提取純化工藝(如目標(biāo)產(chǎn)物去除策略)也各不相同,這些差異直接導(dǎo)致校準(zhǔn)品的組成、對實際樣品的代表性及儲存穩(wěn)定性千差萬別。檢測抗體(尤其是多克隆抗體)需通過免疫動物獲得,其特異性與 HCP 覆蓋度受多重因素影響:免疫原的選擇、動物個體免疫應(yīng)答差異、免疫方案設(shè)計,以及后續(xù)抗體篩選與純化流程,都會讓不同批次或來源的抗體,在對不同 HCP 的親和力、對低豐度蛋白的檢測靈敏度等識別譜特性上,形成本質(zhì)區(qū)別。
E.coli表達菌宿主細胞蛋白(HCP)殘留檢測試劑盒
相關(guān)新聞
- 四川重組藥物支原體檢測驗證菌株 2025-12-08
- 江西干細胞產(chǎn)品支原體檢測培養(yǎng)法 2025-12-08
- 重組藥物支原體檢測快速檢測 2025-12-08
- 北京復(fù)雜基質(zhì)支原體檢測培養(yǎng)法 2025-12-08
- 四川疫苗產(chǎn)品支原體檢測技術(shù)服務(wù) 2025-12-05
- 江蘇CHO宿主細胞蛋白(HCP)殘留檢測試劑盒 2025-12-05
- 浙江疫苗產(chǎn)品支原體檢測指示細胞培養(yǎng)法 2025-12-05
- 廣東免疫細胞產(chǎn)品支原體檢測可比性驗證 2025-12-05
- 重慶重組藥物支原體檢測NAT法 2025-12-05
- 廣東免疫細胞產(chǎn)品支原體檢測國產(chǎn)替代 2025-12-05
推薦新聞
- 靜安區(qū)標(biāo)準(zhǔn)內(nèi)窺鏡工廠直銷 2025-12-08
- 西南國產(chǎn)牙托粉多少錢 2025-12-08
- 海南蛋白分離純化操作細節(jié) 2025-12-08
- 金山區(qū)標(biāo)準(zhǔn)實驗儀器廠家電話 2025-12-08
- 成都點射光纖半導(dǎo)體激光治療儀工廠直銷 2025-12-08
- 江蘇腫瘤術(shù)后菌群檢測常用方法 2025-12-08
- 大量供應(yīng)NAD+誰家生產(chǎn) 2025-12-08
- 崇明區(qū)質(zhì)量實驗儀器專賣店 2025-12-08
- 中國澳門環(huán)保材質(zhì)智能垃圾分類回收秤 2025-12-08
- 上海同濟AKG工廠貼牌 2025-12-08