吉林宿主細胞殘留DNA檢測常用知識
來源:
發布時間:2025-11-05
宿主細胞殘留 DNA 檢測的樣品處理環節,是決定檢測準確性的重要步驟,技術難點貫穿核酸釋放、純化及干擾物去除的全過程。生物制品基質復雜多樣,疫苗、單抗、干細胞、免疫細胞類等不同樣品,對處理方法的要求有較大差異:①疫苗樣品常含甲醛等高濃度滅活劑與鋁鹽等佐劑,易造成 DNA 吸附或降解;②單抗樣品中 10-100 mg/mL 的高蛋白濃度,會競爭性結合磁珠,使提取效率下降;③干細胞與免疫細胞類產品可能殘留二甲基亞砜(DMSO),會直接抑制 PCR 反應。
控制宿主細胞殘留 DNA 含量,對保障生物制品安全性具有重要意義。吉林宿主細胞殘留DNA檢測常用知識
SHENTEK®CV-1殘留DNA檢測試劑盒(PCR-熒光探針法),可對各類生物制品的中間品、半成品及成品中CV-1宿主細胞DNA進行定量檢測。該試劑盒基于熒光探針法原理,實現對樣品中CV-1殘留DNA的定量分析,具備檢測快速、專一性強、性能穩定可靠的特點,檢測限可達到fg級別。試劑盒內配套有CV-1 DNA定量參考品,且與SHENTEK®宿主細胞殘留DNA樣本前處理試劑盒搭配使用,可準確定量樣品中的CV-1殘留DNA。整個分析系統通過優化前處理與檢測步驟的兼容性,能有效提升對CV-1細胞微量DNA殘留的回收率及定量準確度。
北京qPCR法宿主細胞殘留DNA檢測方案對宿主細胞殘留 DNA 檢測方法性能而言,定量限是重要評價指標。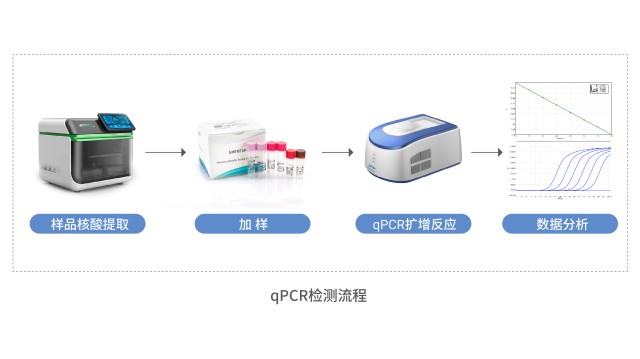
SHENTEK® MRC-5 殘留 DNA 檢測試劑盒,可對各類生物制品中間品、半成品及成品中的 MRC-5 宿主細胞 DNA 進行定量檢測。該試劑盒基于熒光探針原理,實現對樣品中 MRC-5 殘留 DNA 的定量分析,具備檢測速度快、專一性突出、性能穩定可靠的優勢,檢測限可達到 fg 級別,且試劑盒內配備 MRC-5 DNA 定量參考品。該試劑盒與 SHENTEK® 宿主細胞殘留 DNA 樣本前處理試劑盒搭配使用,準確完成樣品中 MRC-5 殘留 DNA 的定量檢測。整個分析系統通過優化前處理與檢測步驟的適配性,提升 MRC-5 細胞微量 DNA 殘留的回收率及定量準確度。
SHENTEK® Sf9&AcNPV 殘留 DNA 檢測試劑盒(多重 PCR - 熒光探針法),可對昆蟲細胞(Sf9)桿狀病毒表達系統所生產的基因工程疫苗中,殘留的 Sf9 細胞 DNA 與桿狀病毒(AcNPV)DNA 進行定量檢測。該試劑盒依托 Taqman 探針原理,結合多重 qPCR 技術實現對樣品中 Sf9 及 AcNPV 殘留 DNA 的定量,不僅檢測效率高、專一性突出,且性能穩定可靠,檢測限可達到 50 copies / 反應,試劑盒還配套提供 Sf9&AcNPV 定量參考品。此試劑盒與 SHENTEK® 宿主細胞殘留 DNA 樣本前處理試劑盒搭配使用,能夠準確定量樣品中殘留的 Sf9&AcNPV 微量 DNA,保障檢測結果的準確性與可靠性。
通過 SHENTEK-96SPCR 儀與湖州申科前處理提取系統的配合,能高效檢測宿主細胞殘留 DNA。
更換宿主細胞殘留DNA(HCD)檢測試劑盒時,需開展一系列驗證相關考量。首先參照《已上市生物制品藥學變更研究技術指導原則(試行)》,根據變更對生物制品安全性、有效性及質量可控性的風險影響程度分類,實施變更前需開展充分研究與驗證。其次進行全面性能驗證,采用藥典方法或已驗證的檢測方法,證明變更后分析方法與原方法等效或更優。隨后開展樣品檢驗,對比試劑盒更換前后的產品質量數據并綜合評估,結合穩定性研究進行穩定性可比性分析,檢測細微差異以評價變更對產品質量的影響。完成上述步驟后,再辦理試劑盒更換備案;若變更后方法與原方法相當或更優,根據待檢樣品為原液或制劑,將變更歸為中等或微小變更,微小變更可在中等變更申請中一并說明。
湖州申科生物為宿主細胞殘留 DNA 檢測提供一站式方案,涵蓋試劑設備及定制化服務。北京E.coli宿主細胞殘留DNA檢測湖州申科圍繞宿主細胞殘留 DNA 檢測,專注于多種生物分析方法的研發優化,遵照法規與指導原則執行。吉林宿主細胞殘留DNA檢測常用知識
疫苗、抗體、重組蛋白、多肽及小分子藥物等產品,多借助連續傳代細胞系進行表達生產。即便經過多步純化工藝處理,終產品中仍可能殘留源自宿主細胞的 DNA(即 Host cell DNA,簡稱 HCD)。HCD 中可能含有功能基因,若其中存在顯性致病基因或病毒基因組,未經驗證、未充分去除或滅活的 HCD 殘留在制品內,可能通過基因層面的隨機插入突變,或是誘發過度 / 異常的免疫原性反應,給用藥者造成不可預測的重大健康風險。由此可見,對宿主細胞殘留 DNA 開展定量檢測,對于監測藥物產品的安全性與質量可控性而言,具有重要意義。
吉林宿主細胞殘留DNA檢測常用知識
下一篇:
江蘇合規性熱原檢測規范
相關新聞
- 江西干細胞產品支原體檢測培養法 2025-12-08
- 重組藥物支原體檢測快速檢測 2025-12-08
- 北京復雜基質支原體檢測培養法 2025-12-08
- 四川疫苗產品支原體檢測技術服務 2025-12-05
- 江蘇CHO宿主細胞蛋白(HCP)殘留檢測試劑盒 2025-12-05
- 浙江疫苗產品支原體檢測指示細胞培養法 2025-12-05
- 廣東免疫細胞產品支原體檢測可比性驗證 2025-12-05
- 重慶重組藥物支原體檢測NAT法 2025-12-05
- 廣東免疫細胞產品支原體檢測國產替代 2025-12-05
- 浙江CHO宿主細胞蛋白(HCP)殘留檢測 2025-12-05
推薦新聞
- 成都點射光纖半導體激光治療儀工廠直銷 2025-12-08
- 江蘇腫瘤術后菌群檢測常用方法 2025-12-08
- 崇明區質量實驗儀器專賣店 2025-12-08
- 中國澳門環保材質智能垃圾分類回收秤 2025-12-08
- 上海同濟AKG工廠貼牌 2025-12-08
- 浙江定做智能假肢廠家 2025-12-08
- 佛山以舊換新助行器價格 2025-12-08
- 浙江NAD+怎么賣 2025-12-08
- 青浦區好的加熱絲回路工廠直銷 2025-12-08
- 青海貨號高鹽核酸酶國內代理 2025-12-08