安徽生物制品支原體檢測核酸擴增法
來源:
發布時間:2025-12-09
湖州申科推出的 MycoSHENTEK® 支原體驗證菌株,符合全球藥典要求,目前已提供口腔支原體、肺炎支原體、豬鼻支原體三種菌株,后續將逐步擴充其他驗證用菌株。該系列菌株溯源至全球保藏機構并獲得正式授權,經培養法測定 CFU(菌落形成單位)與 dPCR 法測定 GC(基因組拷貝數),實現準確定量標定,濃度涵蓋 10CFU 和 100CFU 兩種規格,每盒含 3 管,完全滿足支原體檢測方法驗證需求。菌株經滅活處理,無風險,使用時只需加入相應體積樣品基質即可開展驗證,操作便捷,同時通過雙重定量檢測確保質量可控,為 NAT 方法驗證提供可靠的標準物質支撐。
支原體檢測需驗證專屬性,避免與革蘭氏陽性菌交叉反應,確保結果準確。安徽生物制品支原體檢測核酸擴增法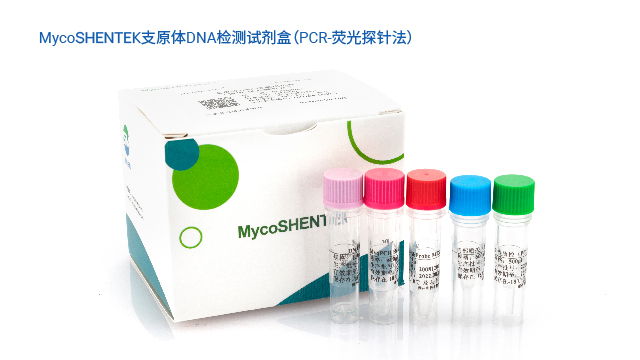
MycoSHENTEK® 支原體 qPCR 檢測試劑盒(2G)完全符合 EP 2.6.7 的全部驗證要求,其檢測靈敏度、特異性、耐用性均按藥典標準完成完整性能驗證,具備替代培養法和指示細胞培養法的合規資質。該試劑盒針對新型生物制品的檢測痛點優化升級,經多種支原體菌株驗證,靈敏度穩定達到 10 CFU/mL,滿足法規對替代培養法的要求。同時,產品遵循 ISO13485 體系認證和 GMP-like 生產標準,可提供完整的驗證報告、質檢報告及菌株溯源文件,全程貼合各國藥典監管要求,為企業合規檢測提供堅實支撐。
免疫細胞產品支原體檢測試劑盒湖州申科支原體驗證菌株溯源至 ATCC/CVCC,標定 10CFU/100CFU,滿足驗證需求。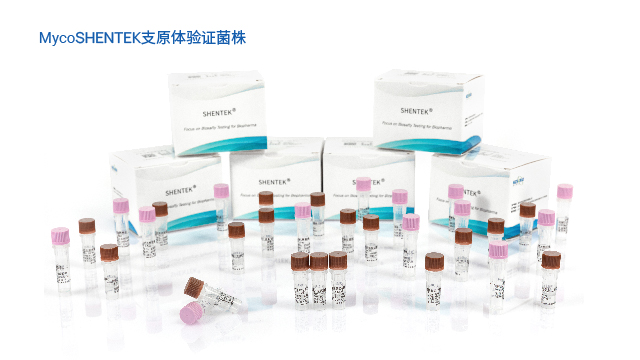
AdvSHENTEK外源因子全自動核酸檢測分析系統以 “迷你 qPCR 實驗室” 的創新形態,突破了傳統支原體檢測的場地限制。整套系統尺寸為 380mm×305mm×343mm,重量只有 14kg,體積小巧、易于部署,無需專門的 PCR 實驗室,只需一間普通實驗室即可滿足檢測需求,大幅降低了企業的場地投入成本。這與傳統 NAT 法需嚴格劃分試劑準備區、樣本制備區、擴增區等多個功能區域的要求形成鮮明對比,尤其適合場地資源緊張的中小企業。同時,系統一體化設計減少了耗材搭配與損耗,自動化流程降低了人為操作失誤導致的重復檢測成本,從場地、人力、耗材多維度為企業實現降本增效,讓支原體檢測更具經濟性。
支原體 NAT 檢測的準確性與可靠性受多重因素綜合影響,需從人員、方法、設備、試劑耗材、實驗室環境五方面嚴格把控。人員需接受專業培訓,熟練掌握 PCR 技術理論與實操流程,積累足夠經驗并具備責任心,確保操作規范性。方法建立需遵循合理流程并完成充分驗證,避免因方法缺陷導致結果偏差。設備方面,PCR 儀與前處理設備的性能、精度、穩定性及定期校準至關重要,直接影響檢測數據的重復性。試劑耗材需滿足要求:前處理試劑能應對復雜樣本基質、耐受常見干擾,檢測試劑經性能驗證且批間穩定性良好,同時需選用質量合格的耗材。實驗室需合理布局,建立完善的管理規范與污染防控措施,為檢測提供潔凈、可控的環境,避免外部因素干擾。
支原體污染來源多樣,包括人源、動物源及環境,需多方位監測。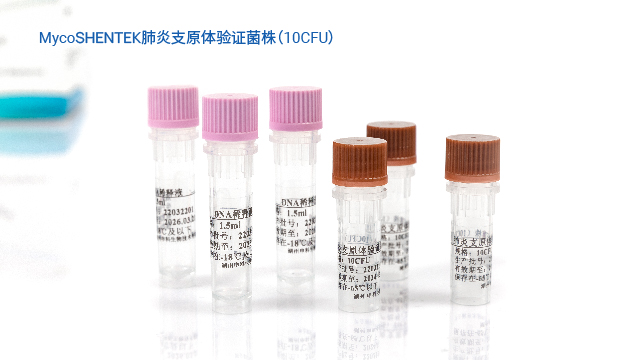
針對新型生物制品中 10?細胞基質、全血、1mg/mL 高濃度質粒、5% 人白等特殊復雜樣品基質,MycoSHENTEK® 支原體 qPCR 檢測試劑盒(2G)進行了方法性能驗證,展現出極強的樣品適用性。實驗數據顯示,在 CHO-S&Vero 細胞(10?個)、5% 人血白蛋白、全血等基質中,該試劑盒對 10 CFU/mL 或 100 CFU/mL 的支原體均能穩定檢出,擴增曲線清晰可靠。其優化的前處理流程與檢測體系有效規避了復雜基質的干擾,無需額外傳代步驟,徹底解決了傳統方法在復雜樣品檢測中易受抑制、結果不準的問題,覆蓋病毒、培養液、成品等多種樣品類型。
實驗室需分區操作支原體檢測,避免陰陽性樣本交叉污染,配備單獨耗材。湖北生物制品支原體檢測指示細胞培養法培養基、血清等原輔料入庫前需做支原體檢測,排除外源污染風險。安徽生物制品支原體檢測核酸擴增法
陰性翹尾是支原體 NAT 檢測中常見的異常現象,表現為 NCS 或 NTC 出現擴增信號,Ct 值多在 35~40 之間,需科學評估并處理。首先考慮污染因素,可能是陰性對照被陽性樣本、試劑或環境氣溶膠污染,建議立即復測,復測時使用帶濾芯低吸附 TIP 頭,嚴格執行陰陽性分區操作,注重細節防控。其次需排除背景信號等非典型性擴增的干擾,避免誤判為污染。若前期驗證中頻繁出現 NTC 或 NCS 擴增,且已徹底排除污染可能性,可結合已有實驗數據重新設置 Cut off 值,確保閾值線能有效區分真實陽性與背景信號,滿足實驗室檢測需求。
安徽生物制品支原體檢測核酸擴增法
上一篇
安徽復雜基質支原體檢測技術服務
下一篇:
重慶疫苗產品支原體檢測技術服務
相關新聞
- 山西熱原檢測方法驗證 2025-12-10
- 福建細胞療法產品支原體檢測試劑盒 2025-12-09
- 廣東干細胞產品支原體檢測國產替代 2025-12-09
- 北京重組蛋白熱原檢測MAT試劑盒 2025-12-09
- 北京細胞療法產品支原體檢測核酸擴增法 2025-12-09
- 吉林復雜基質支原體檢測核酸擴增法 2025-12-09
- 江蘇非動物源熱原檢測規范 2025-12-09
- 福建生物制品支原體檢測指示細胞培養法 2025-12-09
- 重慶疫苗產品支原體檢測培養法 2025-12-09
- 重慶疫苗產品支原體檢測技術服務 2025-12-09
推薦新聞
- 安徽糞便菌群檢測風險預測 2025-12-10
- 靜安區環保切片 2025-12-10
- 便攜式補光儀結構設計 2025-12-10
- 虹口區附近哪里有醫療管理服務策劃 2025-12-10
- 青海國內香囊價格優惠 2025-12-10
- 溫州切片技術指導 2025-12-10
- 高新區附近一次性注射器工廠直銷 2025-12-10
- 國內CD因子表面抗原 2025-12-10
- 需求陽生智能采樣預約管理平臺 2025-12-10
- 陜西國產地巾布巾清洗消毒機價格 2025-12-10