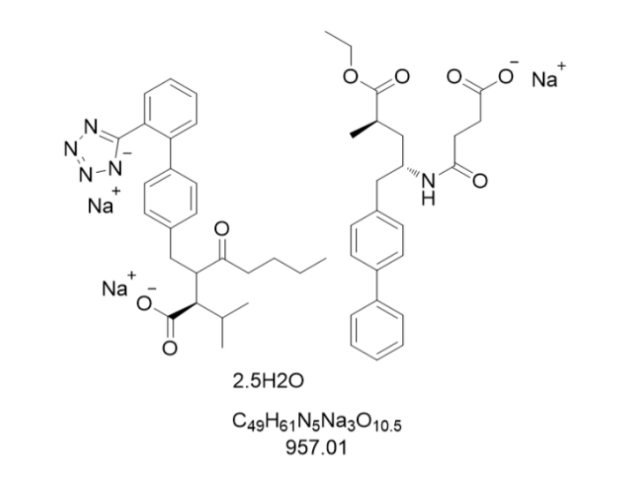
甘肅艾沙佐咪
在聯合醫治性能方面,Ixazomib citrate與免疫調節劑來那度胺及糖皮質物質的協同效應已通過多項Ⅲ期臨床試驗驗證。TOURMALINE-MM1研究顯示,IRd方案(Ixazomib+來那度胺+)較Rd方案(來那度胺+)使中位無進展生存期(PFS)延長10.2個月(20.6 vs 10.4個月),總生存期(OS)達25.8個月,且完全緩解率(CR+VGPR)提升至24.6%。這種療效提升源于多重機制:首先,Ixazomib通過抑制蛋白酶體阻斷NF-κB通路,減少來那度胺耐藥相關細胞因子(如IL-6)的分泌;其次,藥物誘導的未折疊蛋白反應(UPR)可上調來那度胺靶點CRBN的表達,增抵抗力調節作用;通過抑制炎癥因子釋放,緩解Ixazomib誘導的細胞應激反應。安全性分析表明,IRd方案3級以上不良反應發生率與Rd方案相當(62% vs 58%),但外周神經病變發生率明顯降低(28% vs 48%),且無4級神經毒性報告,這主要歸因于Ixazomib的口服給藥的方式減少了靜脈注射相關神經損傷風險。原料藥的出口是許多國家醫藥經濟的重要支柱。甘肅艾沙佐咪
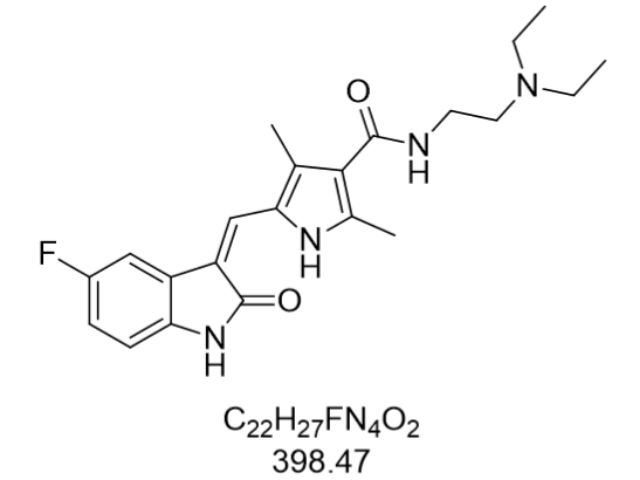
紫杉醇(Paclitaxel,CAS:33069-62-4)作為新一代抗疾病藥物的標志,不僅在醫學領域取得了明顯成就,也推動了藥物研發技術的革新。其獨特的化學結構和作用機制為抗疾病藥物的研發提供了新的思路。在藥物合成方面,紫杉醇的成功制備展示了從天然產物中提取活性成分并通過化學修飾增強其藥效的潛力。紫杉醇的臨床應用還促進了個性化醫療的發展,醫生可以根據患者的具體情況調整用藥劑量和方案,實現精確醫治。隨著生物技術和納米技術的不斷進步,紫杉醇的給藥的方式也在不斷創新,如脂質體紫杉醇的問世,就有效降低了藥物的毒性,提高了醫治的安全性。未來,紫杉醇及其衍生物的研究將繼續深入,為人類抗擊疾病的斗爭貢獻更多力量。卡巴他賽現價原料藥的多晶型現象影響藥物性能。
安全性評估數據顯示,美法侖的毒性特征呈現劑量依賴性與醫治窗狹窄特點。急性毒性研究中,大鼠腹腔LD50為4.484 mg/kg,小鼠皮下LD50為32 mg/kg,提示臨床需嚴格監控血藥濃度。主要不良反應包括骨髓抑制(Ⅲ-Ⅳ度中性粒細胞減少發生率65%)、胃腸道反應(惡心嘔吐發生率40%)和繼發惡性疾病(醫治5年后第二原發疾病風險增加3倍)。特殊人群用藥的方面,老年患者(>65歲)的3-4級不良反應發生率較年輕患者高20%,需進行劑量調整。生殖毒性研究顯示,妊娠期用藥可導致胎兒肢體短缺畸形(發生率約15%),哺乳期婦女用藥后乳汁中藥物濃度可達血藥濃度的30%,因此禁用于妊娠及哺乳期女性。長期隨訪發現,接受累計劑量>200 mg/m2的患者,5年后發生急性髓系白血病的風險為2.3%,這一數據支持臨床采用分次給藥的方案以降低遠期毒性。
5-氨基乙酰丙酸鹽酸鹽,也被稱為5-Aminolevulinic acid HCl,其CAS號為5451-09-2,是一種具有獨特化學和生物活性的有機化合物。它的分子式為C5H10NO3Cl,分子量為167.59。該化合物通常以白色至淡黃色的粉末或結晶形態存在,顯示出良好的水溶性,能夠在二甲基亞砜、甲醇以及水中溶解。5-氨基乙酰丙酸鹽酸鹽在生化研究中占據重要地位,因為它是5-氨基左旋糖酸脫氫酶的底物,并且是天然氨基酸的一種,作為四吡咯的前體,參與葉綠素和血紅素的生物合成過程。它在抗疾病藥物(光敏劑)的開發中扮演著關鍵角色。5-Aminolevulinic acid HCl在體內能代謝形成光敏分子原卟啉(PpIX),當PpIX被光啟動時,會產生具有細胞毒性的活性氧和自由基,這使得5-ALA-HCl成為光動力療法(PDT)中的重要成分,能有效摧毀疾病細胞。值得注意的是,5-氨基乙酰丙酸鹽酸鹽對熱和光敏感,遇熱和光照條件下易分解,因此需在常溫或低溫條件下避光保存。植物提取原料藥從藥用植物中分離活性成分,保留天然藥理特性。
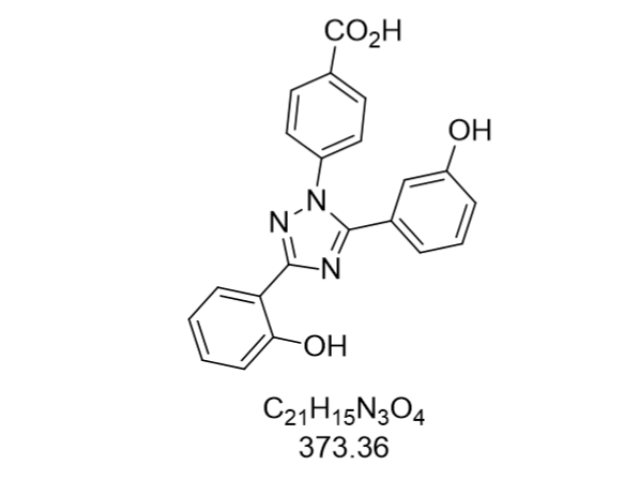
在臨床應用中,Avibactam鈉通過與頭孢他啶聯合使用,構建了廣譜抗細菌組合藥物(如Avycaz?/Zavicefta?),明顯擴大了的覆蓋范圍。該組合對復雜性腹腔內被染(cIAI)、醫院獲得性肺炎(HAP)和呼吸機相關性肺炎(VAP)等重癥被染療效確切。例如,在一項針對銅綠假單胞菌被染小鼠的模型中,Avibactam與頭孢他啶聯合給藥后,頭孢他啶的日劑量可降低2.7至10.1倍,同時維持游離藥物濃度在抑菌閾值(1 mg/L)以上,抑菌率達21.6%(每2小時給藥)和18.5%(每8小時給藥)。此外,Avibactam對產金屬β-內酰胺酶或外排泵高表達的菌株無效,但其與碳青霉烯類(如美羅培南)的聯合方案正在研究中,以應對多重耐藥菌的挑戰。臨床數據顯示,該組合對產KPC酶的肺炎克雷伯菌MIC值隨Avibactam濃度增加呈對數線性下降,凸顯了劑量依賴性增效作用。原料藥市場細分領域機會眾多。甘肅艾沙佐咪
原料藥研發周期長、投入成本高。甘肅艾沙佐咪
在臨床前安全性評估中,德蘭佐米展現出優于傳統蛋白酶體抑制劑的毒性特征。急性毒性實驗顯示,大鼠LD50為120 mg/kg,是硼替佐米(45 mg/kg)的2.7倍。亞慢性毒性研究(28天重復給藥)表明,15 mg/kg劑量組只出現輕度可逆性血小板減少(下降28%),而同等暴露量下硼替佐米會導致45%的血小板減少和30%的神經毒性發生率。機制研究發現,德蘭佐米對正常細胞蛋白酶體的抑制強度只為疾病細胞的1/5,這種差異源于疾病細胞高表達的免疫蛋白酶體(i-proteasome)對其具有更高親和力。在原代人外周血單核細胞(PBMC)中,40 nM濃度處理72小時未誘導明顯凋亡,而相同條件下MM細胞存活率低于5%。更關鍵的是,德蘭佐米不抑制T細胞蛋白酶體活性,反而通過下調PD-L1表達增強T細胞殺傷功能,這種免疫調節特性使其在聯合免疫檢查點抑制劑醫治中具有潛在優勢。目前,該化合物已進入II期臨床試驗(NCT03672218),針對復發/難治性MM患者的初步數據顯示,客觀緩解率達58%,3級以上不良反應發生率較硼替佐米方案降低40%,凸顯其臨床轉化價值。甘肅艾沙佐咪
- 1 2025-12-06
- 紫杉醇側鏈鹽酸鹽(2R 2025-12-06
- 福州5-氨基乙酰丙酸甲酯鹽酸鹽 2025-12-06
- 3-丁烯-1-醇3-Buten-1-ol批發 2025-12-06
- 昆明對甲氧基苯乙胺 2025-12-06
- 西寧甲基琥珀酸酐 2025-12-06
- 二碘-N-乙酰基酪氨酸乙酯生產廠家 2025-12-06
- 3-氨基-4-甲基苯甲酸乙酯Ethyl 3-Amino-4-methylbenzoate廠商 2025-12-05
- 福州4 2025-12-05
- 寧夏N-BOC-L-脯氨醇 2025-12-05
- 廣西智慧手術示教系統供應商 2025-12-07
- 徐匯區推薦吻合器專賣店 2025-12-07
- 青浦區便宜的吻合器銷售廠家 2025-12-07
- 浙江作用助踝器好處 2025-12-07
- 鹽田區質量體外診斷試劑生產企業 2025-12-07
- 上海大腿智能假肢哪家便宜 2025-12-07
- 沙氏葡萄糖培養基使用方法 2025-12-07
- 干旱光合群體光合儀供應商推薦 2025-12-07
- 河北智能步態評估系統 2025-12-07
- 寧波小腿智能假肢多少錢 2025-12-07