中國澳門X射線-熒光雙模態成像系統哪家好
雙模態影像融合精度:解剖與分子的亞微米級配準系統采用基于特征點的配準算法,將X射線與熒光影像的空間偏差控制在2μm以內,確保骨小梁結構與熒光標記細胞的精細對應。在骨轉移*研究中,該精度可識別單個破骨細胞(直徑15μm)與骨小梁微損傷(長度50μm)的空間關系,發現破骨細胞與損傷位點的平均距離<5μm,為“細胞-骨”互作的機制研究提供亞細胞級證據,較傳統配準方法(偏差10μm)更精細揭示分子作用位點。雙模態影像的配準精度達2μm,確保X射線骨結構與熒光標記細胞的空間位置一致性。X射線—熒光雙模態成像系統的參數化報告生成功能,自動輸出骨結構與分子標記的量化指標。中國澳門X射線-熒光雙模態成像系統哪家好

三維重建與動態時序:骨骼疾病的立體認知系統的三維重建軟件可將X射線斷層數據與熒光體積掃描融合,生成骨骼-腫塊的立體模型。在骨關節炎研究中,雙模態三維成像顯示軟骨下骨微骨折區域(X射線低灰度區)與MMP-13熒光標記的基質降解區完全重疊,且通過時序分析發現基質降解先于骨結構改變48小時,為早期干預提供時間窗證據。這種動態立體成像技術,使骨骼疾病的研究從“平面觀察”升級為“時空追蹤”。X射線—熒光雙模態成像系統的骨微CT與熒光顯微的聯合成像,解析骨小梁微結構與細胞分子互作。中國澳門X射線-熒光雙模態成像系統哪家好X射線—熒光雙模態成像系統的骨密度定量分析模塊,結合熒光信號評估成骨細胞功能活性。
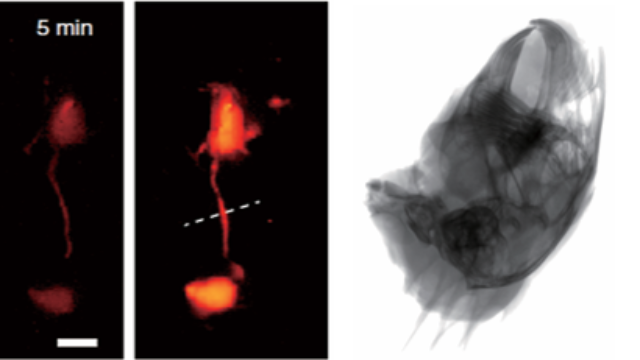
雙模態成像的熱效應評估:激光醫治的安全監控在激光骨消融術中,系統通過X射線實時監測骨組織的熱損傷范圍(如骨密度因熱凝固升高200HU),熒光標記的熱休克蛋白(HSP70探針)顯示細胞損傷程度(熒光強度上升3倍)。該技術將熱損傷邊界的識別精度控制在0.5mm內,避免傳統肉眼判斷的誤差,在動物模型中使激光醫治的骨壞死風險從25%降至3%,為骨科激光手術的安全性提供實時影像監控。高分辨X射線(5μm)與熒光顯微(1μm)的雙模態組合,解析骨小梁微結構與細胞分子互作。
雙模態成像的抗骨轉移藥物篩選:高通量療效評估平臺系統的96孔板適配載物臺支持24只荷瘤小鼠同步雙模態成像,AI算法自動分析X射線的骨破壞面積與熒光的腫塊負荷,24小時內完成80種候選藥物的初步篩選。在臨床前實驗中,該平臺發現某小分子抑制劑可使骨破壞面積減少60%且熒光標記的腫瘤細胞凋亡率提升2.3倍,較傳統單模態篩選效率提升5倍,且能同步評估“抑瘤-護骨”雙重功效,加速抗骨轉移藥物的研發進程。雙模態成像的光譜分離技術,消除X射線散射對熒光信號的干擾,提升數據純凈度。該系統在骨發育研究中通過X射線追蹤骨骼生長板變化,熒光標記生長因子表達動態。
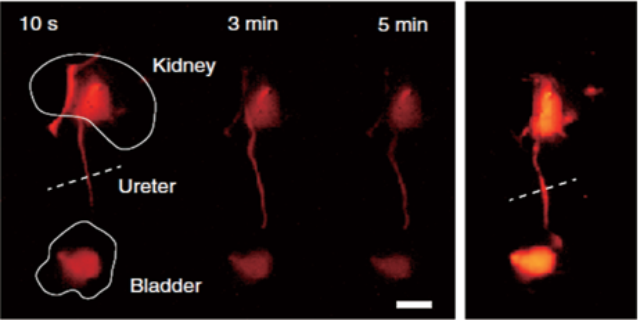
跨模態參數關聯分析:從影像到機制的深度挖掘系統的數據分析模塊可自動計算X射線參數(如骨小梁分離度Tb.Sp)與熒光指標(如凋亡細胞熒光強度)的相關性,在骨質疏松性骨折模型中發現Tb.Sp與成骨細胞凋亡率的相關系數r=0.85。這種跨模態關聯分析可深入挖掘影像數據背后的生物學機制,例如通過X射線的骨微結構異常預測熒光標記的細胞凋亡通路***,為骨疾病的早期預警與干預提供分子層面的理論依據。 X射線—熒光雙模態成像系統的無線數據傳輸功能,支持手術間與實驗室的實時影像共享。該系統在骨質疏松研究中通過X射線量化骨密度,熒光標記成骨細胞活性動態。遼寧X射線-熒光X射線-熒光雙模態成像系統哪家好
該系統的雙模態數據管理平臺支持多時間點影像的縱向對比與量化分析。中國澳門X射線-熒光雙模態成像系統哪家好
雙模態影像的科普可視化:加速科研成果轉化系統生成的3D融合影像(X射線骨結構透明化+熒光分子標記偽彩)可直觀展示骨骼疾病的發生機制,如骨轉移*的“溶骨-成骨”混合病灶與腫瘤細胞浸潤路徑。這種可視化素材適用于學術匯報、科普教育及臨床醫患溝通,例如向患者展示X射線所示的骨破壞區域與熒光標記的腫塊活性區,幫助理解治療方案的制定依據,較傳統二維影像的溝通效率提升70%,促進科研成果向臨床應用的轉化。 雙模態同步掃描技術將X射線與熒光成像的時間偏差控制在50ms內,確保動態過程一致性。中國澳門X射線-熒光雙模態成像系統哪家好
- 黑龍江X射線-熒光X射線-熒光雙模態成像系統哪里有賣的 2025-11-27
- 西藏近紅外二區顯微成像系統品牌排行 2025-11-27
- 上海近紅外二區熒光壽命成像系統解決方案 2025-11-27
- 河北近紅外二區全光譜小動物活體成像系統回收價 2025-11-27
- 浙江X射線-熒光近紅外二區熒光壽命成像系統設計 2025-11-27
- 上海熒光全光譜小動物活體成像系統常用知識 2025-11-27
- 中國香港近紅外二區X射線-熒光雙模態成像系統廠家直銷 2025-11-27
- 江西近紅外二區顯微成像系統推薦廠家 2025-11-27
- 中國香港成像系統近紅外二區熒光寬場成像系統維保 2025-11-27
- 河南全光譜小動物成像系統歡迎選購 2025-11-27
- 深圳壓力傳感器私人定做 2025-12-10
- 貴州本地西門子PLC 2025-12-10
- 杭州工業車速傳感器直銷價格 2025-12-10
- 江蘇單槽基因擴增儀PCR儀一般多少錢 2025-12-10
- 浦東新區品牌電子產品維保 2025-12-10
- 泵類振動巡測儀 2025-12-10
- 上海地鐵信息化軟件與平臺 2025-12-10
- 江蘇如何選智能差壓變送器生產企業 2025-12-10
- 迅杰光遠IAS-3120玉米胚芽檢測儀器多少錢 2025-12-10
- 安徽PR-Xv30單組份點膠售后服務 2025-12-10