江蘇外包科研技術服務購買
外泌體的抑制作用外泌體水平升高通常與不同類型的惡化相關,一些研究人員希望能通過降低外泌體到正常水平來防止不良預后。從這個角度出發,許多正在進行的研究旨在通過調節外泌體生成分泌的過程或通過特異性靶向其成分抑制其與靶細胞的相互作用來調節外泌體的產生。如今我們對外泌體機制和不同生理和病理條件下的功能的理解呈指數級增長,雖然目前其生物學功能還未完全解析清楚,但研究者們在許多領域均已對其進行了深入探索。外泌體不是廢物顆粒,而是細胞間通訊的關鍵介質,作為宿主細胞的衛星,外泌體包含大量的生物信息,其功能超出了初的預期,宿主細胞控制著外泌體的內容物,從而改變了自己或其他細胞的命運。其次,外泌體對的進展和轉移有著強烈的影響,可以通過外泌體預測轉移的部位并建立轉移前的生態位。參考文獻:[1]高方園,焦豐龍,張養軍,秦偉捷,錢小紅.外泌體分離技術及其臨床應用研究進展[J].色譜,2019,37。實驗干貨 | 分子克隆實驗——無縫克隆。江蘇外包科研技術服務購買
METTL3能夠促進肺腺細胞的生長、生存和侵襲,但還不清楚它是否作為m6A調節器或效應器發揮作用[25]。在急性髓細胞白血病(AML)患者中,m(6)A調控基因的突變或拷貝數變化與TP53突變存在密切聯系,且m(6)A調控基因的改變與AML不良預相關[26]。此外,FTO在AML中高表達,它通過降低mRNA轉錄本中的m(6)水平,調節ASB2和RARA等靶點的表達,增強了白血病基因介導的細胞轉化和白血病形成,并抑制全反式維甲酸(ATRA)誘導的AML細胞分化[27]。在脂肪形成過程中,FTO表達與m6A水平成負相關,促進脂肪形成[3]。在膠質細胞瘤樣細胞中,ALKBH5通過lncRNAFOXM1介導FOXM1基因pre-mRNA上的m6A修飾維持膠質瘤細胞的成瘤性[28]。此外,甲基轉移酶METTL3或METTL14的敲除,能夠改變m6A的富集和ADAM19的表達,極大地促進了膠質瘤細胞的生長、自我更新和形成[29]。圖2m6ARNA修飾和介導的功能[30]m6A的研究方向主要是通過研究m6A修飾相關的甲基化、去甲基化酶和識別蛋白的功能,進而研究m6A修飾的生物學功能和作用機制:一般通過敲除m6A酶分子,研究下游功能基因分子的表達和m6A甲基化情況,通過介導相關基因異常(可變剪切、穩定性、翻譯、miRNA調控)影響細胞表型和功能特征。海南科研技術服務分離建立疾病模型的目的是為了防治人類疾病。
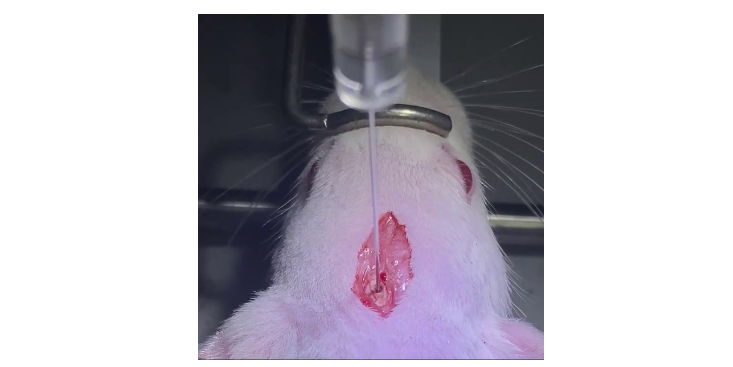
如胰腺,一般取胰島較多的胰腺尾部;肺應取有細支氣管及帶有軟骨片的小支氣管部。如果實驗需進行多樣本的采集,采集順序應按照:消化,神經系統,皮膚,肌肉等的順序進行。選好塊的切面。熟悉某些成分安排,然后決定其切面的走向;如一長管狀以橫切面較好。切除不需要的部分。特別是周圍的脂肪等,應盡可能掉,否則給固定、脫水、浸蠟、切片等帶來一些不必要的問題。樣品的固定(1)固定的方法:①小塊固定法:從動物取下的小塊,立即置入液態固定劑(這是應用經常的方法)。②注射/灌注固定法:某些塊由于體積過大或固定液極難滲入內部或需要對整個臟器或整個動物進行固定,這時宜采用注射固定法,將固定液注入血管,經血管分支到達整個和全身,從而得到充分的固定。另,空腔比如肺,肺內含有空氣,固定液難以滲入,建議先做肺灌注,使得肺充盈滿固定液以后再進行保存,如果空腔中氣體沒有排出,后續可能影響固定效果(沒有灌注的肺會浮在液體表面不利于固定,切片以后也會看到很多的空泡)。③蒸汽固定法:比較細小而薄的標本,可用鋨酸或甲醛蒸汽固定。主要用于血液或細胞涂片以及某些薄膜的固定。。
注意事項1.病毒包裝的幾個關鍵點主要包括:細胞因素、載體系統(盡量使用成熟的商業化載體系統)、構建重組的質粒正確與否、質粒抽提純化情況、包裝轉染控制(24、48小時的細胞及熒光狀態判斷)、目的基因對病毒包裝影響(基因大小、序列情況、蛋白功能毒性等都會影響到是否能包裝成功)。,需要觀察包裝病毒后的48h培養基顏色是否橙紅。3.病毒濃縮:病毒一般在48h和72h各收一次。如果不想濃縮病毒的話,也可以直接將收集的病毒上清作為要的細胞的培養基,但是可能效果會不太好。并且一般收病毒時,培養基的營養已經損耗了很多,那樣直接培養細胞會損害細胞,所以建議還是進行濃縮后再。常見問題1.包裝病毒時293T細胞狀態不好,或者鋪得過密,可以選擇放棄該次實驗。2.目的載體過大,不易。3.避免轉染過程以及后續過程出現的污染。動物疾病模型可以分為兩種類型:自然模型和人工模型。
RNA甲基化修飾(m6A)研究RNA甲基化修飾約占所有RNA修飾的60%以上,而N6-甲基腺嘌呤(N6-methyladenosine,m6A)是高等生物mRNA和lncRNAs上為普遍的修飾。目前發現microRNA,circRNA,rRNA,tRNA和snoRNA上都有發生m6A修飾。m6A修飾主要發生在RRACH序列中的腺嘌呤上,其功能由“編碼器(Writer)”、“消碼器(Eraser)”和“讀碼器(Reader)”決定[1]。“編碼器(Writer)”即甲基轉移酶,目前已知這個復合物的成分有METTL3,METTL14,WTAP和KIAA1429;而ALKBH5和FTO作為去甲基酶(消碼器)可逆轉甲基化;m6A由m6A結合蛋白識別,目前發現m6A結合蛋白(讀碼器)有YTH結構域蛋白(包括YTHDF1,YTHDF2,YTHDF3,YTHDC1和YTHDC2)和核不均一蛋白HNRNP家族(HNRNPA2B1和HNRNPC)。m6A酶系統METTL3是早先被鑒定為結合SAM的組件,其缺失引起小鼠胚胎干細胞、Hela細胞和HepG2細胞中m6Apeaks的減少。METTL3及其同源蛋白METTL14定位在富含剪切因子的細胞核內亞細胞器-核小斑(Nuclearspeckle)上,顯示m6A修飾可能和RNA的剪切加工相關。WTAP與METTL3–METTL14二聚體相互作用,并共定位于核小斑,影響甲基化效率,參與mRNA剪。而KIAA1429作為候選的甲基轉移酶復合體的新亞基。實驗技巧——做好細胞凍存,保證細胞質量。浙江裸鼠科研技術服務外包
健康的HEK 293T細胞,一般使用復蘇后10代以內的細胞進行慢病毒的生產,要求無菌以及支原體污染;江蘇外包科研技術服務購買
建立疾病模型的目的是為了防治人類疾病。因此,疾病模型研究結果的可靠程度取決于模型與人類疾病的相似或可比擬的程度。接下來就讓上海研錄帶您了解相關知識。一個好的疾病模型應具有以下特點:①能夠再現所要研究的人類疾病,動物疾病表現應該與人類疾病相似;②動物能重復產生該疾病,盡可能能在兩種動物體內復制該病;③動物背景資料完整,實驗動物合格,生命周期要滿足實驗需要;④動物要價廉、來源充足、便于運送;⑤盡可能選用小動物。生物醫學科研專業設計中常要考慮如何建立動物模型的問題,因為很多闡明疾病及療效機制的實驗不可能或不應該在患者身上進行。常要依賴于復制動物模型,但一定要進行周密設計,設計時要遵循下列一些原則:(一)相似性在動物身上復制人類疾病模型,目的在于從中找出可以推演應用于患者的有關規律。外推法(extrapolation)要冒風險,因為動物與人到底不是一種生物。如,在動物身上無效的藥物不等于臨床無效,反之亦然。因此,設計動物疾病模型的一個重要原則是,所復制的模型應盡可能近似于人類疾病的情況。能夠找到與人類疾病相同的動物自發性疾病當然是比較好的。(二)重復性理想的動物模型應該是可重復的,甚至是可以標準化的。如。江蘇外包科研技術服務購買
- 湖北原代細胞服務 2025-12-06
- 組織原代細胞實驗 2025-12-06
- 寧夏裸鼠原代細胞技術 2025-12-06
- 吉林血液原代細胞 2025-12-06
- 上海組織科研技術服務培養 2025-12-06
- 湖北血液科研技術服務技術 2025-12-06
- 基因敲除動物模型造模 2025-12-06
- 湖北哪里有科研技術服務技術 2025-12-06
- 模式原代細胞外包 2025-12-06
- 山西實驗科研技術服務技術 2025-12-06
- 六盤水2025年專精特新認定價格信息 2025-12-06
- 化妝品包裝設計營銷戰略 2025-12-06
- 上海本地禮儀服務聯系方式 2025-12-06
- 青浦區一站式文化藝術活動策劃平臺 2025-12-06
- 杭州拱墅區尋釁滋事刑事辯護監外執行 2025-12-06
- 奉賢區提供舞臺設備銷售便捷 2025-12-06
- 泉州機加工勞務派遣公司推薦 2025-12-06
- 廣東哪里電商配送服務方案 2025-12-06
- 太原創新型企業服務中心數實融合趨勢 2025-12-06
- 廣東大堂室內裝修工藝 2025-12-06